Nowatorski antybiotyk opracowany na Uniwersytecie Waszyngtońskim leczy ciężkie infekcje u myszy i jest obiecujący w walce z lekoopornymi bakteriami. Związek przyspiesza gojenie i już wkrótce może wejść do badań klinicznych, których celem będzie dostarczenie nowego rozwiązania w walce z chorobami bakteryjnymi.
Nowy antybiotyk opracowany przez naukowców z Washington University skutecznie leczy ciężkie infekcje bakteryjne, w tym choroby mięsożerne, u myszy.
Badanie, które wskazuje na szerokie spektrum działania przeciwko bakteriom lekoopornym, pokazuje, że związek ten pomaga również w szybszym powrocie do zdrowia i zmniejszeniu ciężkości infekcji. Zanim jednak lek trafi na rynek, wymagane są szeroko zakrojone testy i badania kliniczne.
Przełom w badaniach nad antybiotykami
Naukowcy z Washington University School of Medicine w St. Louis opracowali nowy związek, który skutecznie usuwa infekcje bakteryjne u myszy, w tym te, które mogą powodować rzadkie, ale potencjalnie śmiertelne choroby „mięsożerne”. Związek ten może być pierwszym z zupełnie nowej klasy antybiotyków i prezentem dla klinicystów poszukujących skuteczniejszych metod leczenia bakterii, których nie można łatwo oswoić za pomocą dostępnych antybiotyków.
Wyniki badania opublikowano dzisiaj (2 sierpnia) w czasopiśmie Postęp nauki.
Związek celuje w bakterie Gram-dodatnie, które mogą powodować lekooporne zakażenia gronkowcem, zespół wstrząsu toksycznego i inne choroby, które mogą okazać się śmiertelne. Został opracowany dzięki współpracy laboratoriów dr Scotta Hultgrena, profesora mikrobiologii molekularnej Helen L. Stoever i dr Michaela Caparona, profesora mikrobiologii molekularnej, oraz Fredrika Almqvista, profesora chemii na Uniwersytecie w Umeå w Szwecji.
Nowy rodzaj środka przeciwdrobnoustrojowego byłby dobrą wiadomością dla klinicystów poszukujących skutecznych metod leczenia patogenów, które stają się coraz bardziej oporne na obecnie dostępne leki, a przez to znacznie bardziej niebezpieczne.
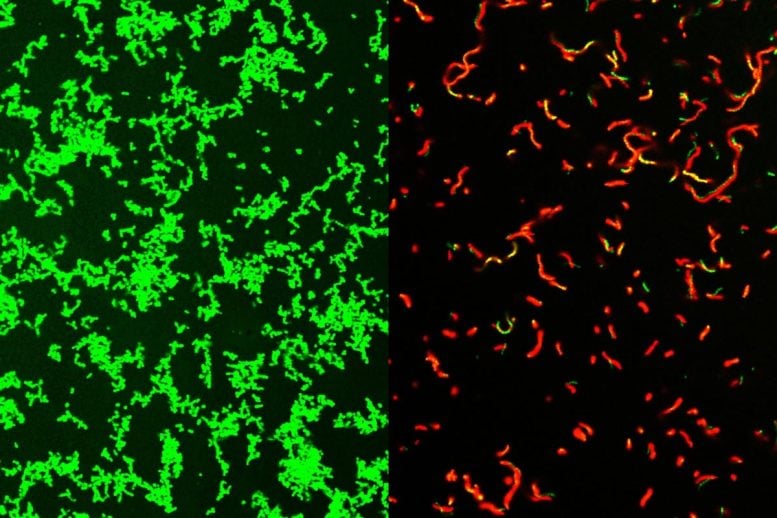
Naukowcy z Washington University School of Medicine w St. Louis opracowali związek skuteczny przeciwko powszechnym bakteriom, które mogą prowadzić do rzadkich, niebezpiecznych chorób. Na tym zdjęciu widać, że nie jest leczony Streptococcus pyogenes kultura bakteryjna pełna zdrowych drobnoustrojów, oznaczona na zielono (po lewej). Po obróbce za pomocą GmPcide naczynie jest pełne martwych bakterii (czerwone; po prawej). Źródło: dr Zongsen Zou, Washington University w St Louis
Działanie przeciwdrobnoustrojowe o szerokim spektrum działania
„Wszystkie bakterie Gram-dodatnie, które testowaliśmy, były wrażliwe na ten związek. Obejmuje to enterokoki, gronkowce, paciorkowce, C. trudne, które są głównymi typami bakterii chorobotwórczych” – powiedział Caparon, współautor. „Związki mają szerokie spektrum działania przeciwko licznym bakteriom”.
Opiera się na typie cząsteczki zwanej 2-pirydonem skondensowanym z pierścieniem. Początkowo Caparon i Hultgren poprosili firmę Almqvist o opracowanie związku, który mógłby zapobiegać przyleganiu błony bakteryjnej do powierzchni cewników cewki moczowej, co jest częstą przyczyną szpitalnych infekcji dróg moczowych. Odkrycie, że powstały związek ma właściwości zwalczające infekcje przeciwko wielu typom bakterii, było szczęśliwym przypadkiem.
Zespół nazwał swoją nową rodzinę związków GmPcides (dla środka Gram-dodatniego). W poprzednich pracach autorzy wykazali, że GmPcides może zniszczyć szczepy bakterii w eksperymentach na płytce Petriego. W najnowszym badaniu postanowiono przetestować go na martwiczych infekcjach tkanek miękkich, które są szybko rozprzestrzeniającymi się infekcjami, zwykle z udziałem wielu typów bakterii Gram-dodatnich, dla których Caparon miał już działający mysi model. Najbardziej znana z nich, martwicze zapalenie powięzi lub „choroba mięsożerna”, może szybko uszkodzić tkankę na tyle poważnie, że konieczna będzie amputacja kończyny w celu kontrolowania jej rozprzestrzeniania się. Około 20% pacjentów z chorobą mięsożerną umiera.
Implikacje kliniczne
W badaniu tym skupiono się na jednym patogenie, Streptococcus pyogenes, która co roku jest odpowiedzialna za 500 000 zgonów na całym świecie, w tym choroby mięsożerne. Myszy zakażone S. pyogenes i leczone GmPcide radziły sobie lepiej niż nieleczone zwierzęta pod niemal każdym względem. Miały mniejszą utratę wagi, owrzodzenia charakterystyczne dla infekcji były mniejsze i szybciej walczyły z infekcją.
Okazało się, że związek zmniejsza zjadliwość bakterii i, co niezwykłe, przyspiesza gojenie uszkodzonych obszarów skóry po infekcji.
Nie jest jasne, w jaki sposób GmPcides osiąga to wszystko, ale badanie mikroskopowe ujawniło, że leczenie wydaje się mieć znaczący wpływ na błony komórkowe bakterii, które stanowią zewnętrzną osłonę drobnoustrojów.
„Jednym z zadań membrany jest oddzielanie materiału od zewnątrz” – powiedział Caparon. „Wiemy, że w ciągu pięciu do dziesięciu minut po zastosowaniu GmPcide błony zaczynają stać się przepuszczalne i umożliwiają przedostanie się do bakterii substancji, które normalnie powinny być wykluczone, co sugeruje, że błony te zostały uszkodzone”.
Może to zakłócić własne funkcje bakterii, w tym te, które powodują szkody u żywiciela, i sprawić, że bakterie będą mniej skuteczne w zwalczaniu odpowiedzi immunologicznej żywiciela na infekcje.
Wyzwania i przyszłość
Oprócz swojej skuteczności przeciwbakteryjnej wydaje się, że GmPcides rzadziej powodują powstawanie szczepów lekoopornych. Eksperymenty mające na celu stworzenie opornych bakterii wykazały, że bardzo niewiele komórek jest w stanie wytrzymać leczenie i tym samym przekazać swoje zalety kolejnym pokoleniom bakterii.
Caparon wyjaśnił, że przed nami jeszcze długa droga, zanim GmPcides prawdopodobnie trafią do lokalnych aptek. Caparon, Hultgren i Almqvist opatentowali związek wykorzystany w badaniu i udzielili licencji na niego firmie QureTech Bio, w której mają udziały, oczekując, że będą mogli współpracować z firmą, która jest w stanie zarządzać prace nad rozwojem farmaceutycznym i badaniami klinicznymi, które mogą potencjalnie wprowadzić GmPcides na rynek.
Hultgren powiedział, że rodzaj współpracy naukowej, która doprowadziła do powstania GmPcides, jest potrzebny do leczenia nierozwiązywalnych problemów, takich jak oporność na środki przeciwdrobnoustrojowe.
„Wszelkie infekcje bakteryjne stanowią ważny problem zdrowotny i stają się coraz bardziej odporne na wiele leków, a przez to trudniejsze w leczeniu” – stwierdził. „Nauka interdyscyplinarna ułatwia integrację różnych dziedzin nauki, co może prowadzić do nowych, synergicznych pomysłów, które mogą pomóc pacjentom”.
Odniesienie: „2-pirydonowe związki przeciwdrobnoustrojowe ze skondensowanymi pierścieniami dihydrotiazolowymi leczą zakażenia skóry i tkanek miękkich Streptococcus pyogenes” 2 sierpnia 2024 r., Postęp nauki.
DOI: 10.1101/2024.01.02.573960