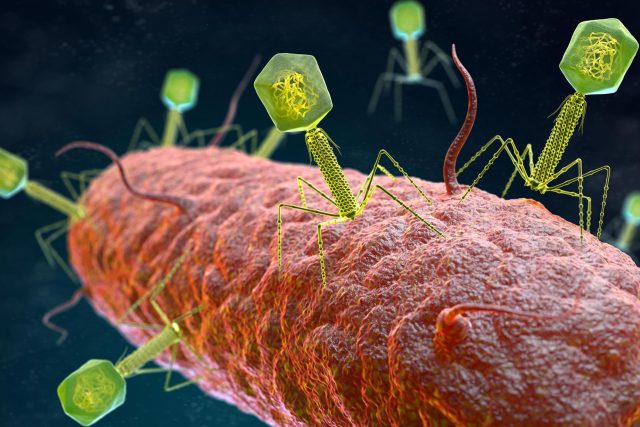
Nowe badanie pokazuje, jak singiel gatunek bakterii może utrzymać zróżnicowaną społeczność gatunków fagów, co ma wpływ na projektowanie skutecznych terapii fagowych.
Naukowcy z Uniwersytetu Nowojorskiego, Oksfordu i Yale wykazali, że fagi mogą współistnieć, wykorzystując różne tempo wzrostu w populacji bakterii, co sugeruje, że wiele fagów można stosować razem, aby zapobiec rozwojowi oporności.
Wirusowe „życie społeczne” kluczem do opracowania metod leczenia infekcji bakteryjnych za pomocą fagów
Wirusy infekujące i zabijające bakterie, zwane fagami, są obiecujące w leczeniu niebezpiecznych infekcji, w tym szczepów opornych na antybiotyki. Jednak naukowcy nadal niewiele wiedzą na temat sposobu, w jaki fagi przeżywają w populacjach bakterii, co utrudnia opracowanie skutecznych terapii opartych na fagach.
Badanie opublikowane dzisiaj (12 grudnia) w czasopiśmie Nauka dostarcza pierwszego dowodu na to, że pojedynczy gatunek bakterii może wspierać zróżnicowaną społeczność konkurujących ze sobą fagów. Naukowcy z NYU Grossman School of Medicine w Oksfordzie i Uniwersytet Yale’a odkryli, że w genetycznie identycznym szczepie może współistnieć wiele gatunków fagów E. colibakteria powszechnie występująca w ludzkich jelitach, która obejmuje zarówno nieszkodliwe, jak i chorobotwórcze warianty.
Mechanizmy różnorodności fagów
Naukowcy odkryli, że pomimo konkurencji między wirusami różne gatunki fagów preferowały wolniej lub szybciej rosnące komórki, które losowo pojawiały się w populacji. W ten sposób każdy gatunek faga był w stanie znaleźć odrębną niszę na tym samym gospodarzu, co doprowadziło do stabilnego współistnienia.
Na przykład brak lokalnego dostępu do składników odżywczych (głód) może spowolnić wzrost niektórych komórek w celu zachowania ograniczonych zasobów. W bieżącym badaniu dwa gatunki fagów, oznaczone N i S, współistniały, ponieważ N był lepiej przystosowany do przeżycia w szybko rosnących komórkach bakteryjnych, podczas gdy fag S był lepszy w wolno rosnących komórkach.
Projektowanie skutecznych terapii fagowych
Twórcy terapii fagowych mają nadzieję zażegnać problem w leczeniu antybiotykami, gdzie określony lek zabija bakterie, ale pozostawia przy życiu tę frakcję, która przez przypadek jest najbardziej odporna na mechanizm działania leku. Osoby, które przeżyły, stanowią poważny problem, ponieważ stały się odporne na dostępne metody leczenia.
„Wiedza, w jaki sposób więcej niż jeden rodzaj fagów może przetrwać w czasie na pojedynczej bakterii, może pomóc w projektowaniu koktajli fagów nowej generacji” – powiedziała autorka pierwszego badania Nora Pyenson, doktorantka w laboratorium współautora Jonasa Schluter, dr hab Instytut Genetyki Systemów w NYU Langone Health. „Na przykład każdy gatunek faga może zaatakować bakterię w innej części jej cyklu życiowego, umożliwiając zabicie całej populacji, zanim rozwinie się oporność na leczenie”.
„Żadne terapie fagowe nie stały się jeszcze standardowym sposobem leczenia infekcji bakteryjnych, albo dlatego, że w poprzednich próbach pojedynczy fag nie zabił wszystkich docelowych bakterii, albo dlatego, że bakterie ewoluowały, aby uodpornić się, podobnie jak ewolucja oporności na antybiotyki” – dodaje dr Pyenson .
Terapia fagowa w badaniach klinicznych
Laboratoria testują już leczenie fagami jako alternatywę dla antybiotyków. Na przykład współautor aktualnej pracy, doktor Paul Turner z Uniwersytetu Yale, prowadzi badanie kliniczne z wykorzystaniem fagów przeciwko gatunkowi Pseudomonas aeruginosaktóre mogą przyczyniać się do ciężkiego stanu zapalnego w płucach pacjentów z mukowiscydozą. Laboratorium dr Schlutera bada rolę fagów w ekosystemie jelitowym ludzi i myszy, która może kształtować przyszłe terapie takich infekcji jak Salmonella. Głównym celem jest przewidywanie wpływu podawania fagów i zaprojektowanie terapii fagowych, które w przeciwieństwie do obecnych wersji, które muszą być dostosowane do konkretnego pacjenta, będą działać uniwersalnie u wielu pacjentów.
Ekologia fagów i różnorodność wirusów
Zrozumienie różnorodności gatunków jest fundamentalnym pytaniem w ekologii i biologii ewolucyjnej. Głównym czynnikiem umożliwiającym różnorodność, od ptaków, przez rośliny, po bakterie, jest to, że gatunki znajdują sposoby na współistnienie, jednocześnie konkurując o zasoby. Jednakże wirusy nie były tradycyjnie postrzegane w tym kontekście „społecznym”.
Obecny zespół badawczy eksperymentalnie przetestował długo utrzymywane założenie, że różnorodność genetyczna bakterii ogranicza różnorodność gatunków wirusów. Prowadziło to do oczekiwania, że jeden typ faga prześcignie wszystkie inne i zostanie jedynym typem faga, który przeżyje. Jednakże, podobnie jak organizmy wielokomórkowe są gospodarzami szerokiej gamy gatunków bakterii w swoim mikrobiomie, nowe wyniki pokazują, że pojedynczy szczep bakteryjny może sam w sobie być gospodarzem zróżnicowanej społeczności gatunków fagów.
„Nasze badanie wnosi wkład w rozwijającą się dziedzinę badań nad życie społeczne wirusów” – dodaje dr Pyenson. „Często myślimy o wirusach wyłącznie w kategoriach ich wpływu na żywiciela, ale istnieją one również w kontekście innych gatunków wirusów. Te społeczności fagów pokazują, jak różnorodność pojawia się nawet wśród najprostszych fragmentów biologii”.
Wpływ na zdrowie i chorobę
Co ciekawe, obecność zróżnicowanej populacji bakterii w jelitach człowieka jest oznaką zdrowia, ponieważ zróżnicowany zestaw gatunków (mikrobiom) jest w stanie lepiej przeciwstawić się próbom dominacji ze strony wszelkich inwazyjnych gatunków chorobotwórczych. Z tego samego powodu populacja wirusów zamieszkujących bakterie żyjące w jelitach również staje się ważnym regulatorem zdrowia, przy czym uważa się, że nieprawidłowe mieszaniny fagów przyczyniają się do chorób takich jak posocznica.
„Ta praca reprezentuje zmianę w naszym rozumieniu ekologii fagów” – powiedział dr Schluter, także profesor na Wydziale Mikrobiologii Uniwersytetu Nowojorskiego w Langone. „Dzięki pracy Nory, którą przeprowadziła przez pandemię i w czterech laboratoriach, możemy teraz zacząć rozumieć ewolucję fagów, gdy żyją w społeczności z różnymi gatunkami wirusów, oraz jak kształtuje to ich rolę w zdrowiu i chorobie”.
Odniesienie: „Dynamika społeczności fagów i ekologia na klonalnym gospodarzu bakteryjnym” 12 grudnia 2024 r., Nauka.
DOI: 10.1126/science.adk1183
Wraz z dr. Pyenson i Schluter z NYU Langone oraz dr Turner z Yale, autorami badania byli Asher Leeks i Odera Nweke z Wydziału Ekologii i Biologii Ewolucyjnej Uniwersytetu Yale; Joshua Goldford w Zakładzie Nauk Geologicznych i Planetarnych w California Institute of Technology w Pasadenie; Kevin Foster z Wydziału Biologii Uniwersytetu im Uniwersytet Oksfordzki; oraz Alvaro Sanchez z Instytutu Biologii Funkcjonalnej i Genomiki, CSIC i Uniwersytetu w Salamance w Hiszpanii. dr. Foster i Sanchez byli autorami korespondującymi obok doktora Pyensona.
Część prac została sfinansowana przez Life Science Research Foundation i Fundację Simonsa dr Pyensonowi, a także przez nagrodę New Innovator Award dla dr Schlutera (DP2AI164318) z Narodowego Instytutu Chorób Autoimmunologicznych i Zakaźnych, będącej częścią projektu Narodowe Instytuty Zdrowia.