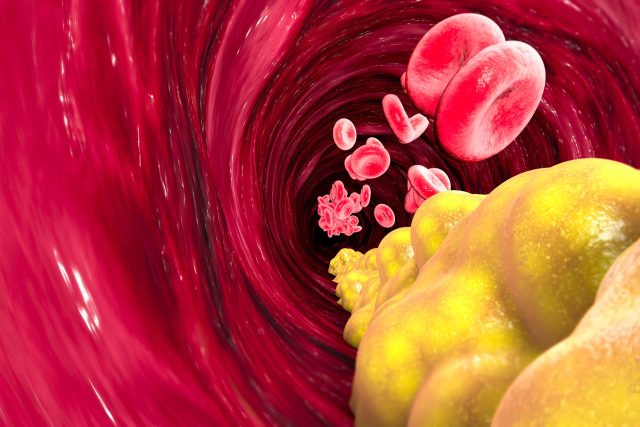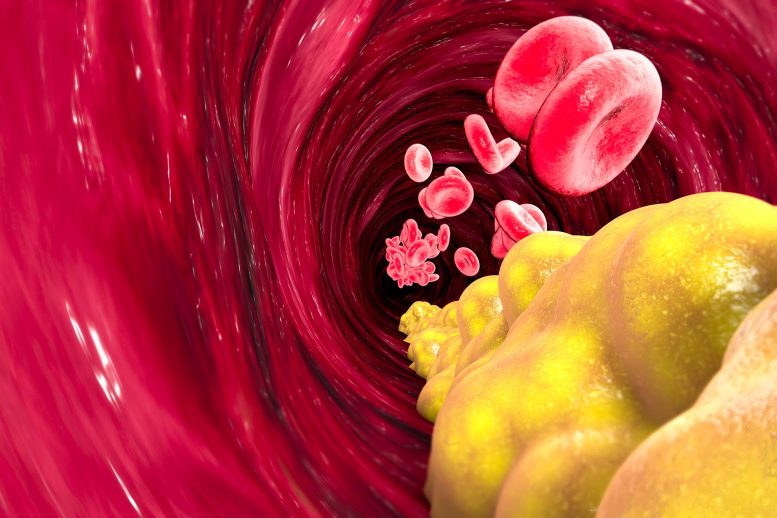
Odkrycia mogą pomóc w opracowaniu bardziej dostosowanych metod leczenia choroba sercowo-naczyniowa.
Naukowcy z Narodowe Instytuty Zdrowia (NIH) osiągnęli kamień milowy w zrozumieniu mechanizmów stojących za akumulacją „złego” cholesterolu, czyli cholesterolu lipoprotein o małej gęstości (LDL-C), w organizmie. Po raz pierwszy naukowcy wykazali, w jaki sposób podstawowe białko strukturalne LDL oddziałuje ze swoim receptorem, inicjując proces usuwania LDL z krwiobiegu. Zidentyfikowali także konsekwencje zakłóceń w tym procesie.
Opublikowano w Naturaodkrycia poszerzają naszą wiedzę na temat wpływu LDL na choroby serca – główną przyczynę zgonów na świecie – i mogą utorować drogę dla bardziej dostosowanych terapii obniżających poziom LDL, takich jak spersonalizowane leczenie statynami, w celu poprawy ich skuteczności.
Związek między LDL a chorobami sercowo-naczyniowymi
„LDL jest jednym z głównych czynników powodujących choroby układu krążenia, które co 33 sekundy zabijają jedną osobę, więc jeśli chcesz zrozumieć swojego wroga, chcesz wiedzieć, jak on wygląda” – powiedział Alan Remaley, lekarz medycyny, współwłaściciel – starszy autor badania, prowadzący Laboratorium Metabolizmu Lipoprotein w Narodowym Instytucie Serca, Płuc i Krwi NIH.
Do tej pory naukowcy nie byli w stanie wyobrazić sobie struktury LDL, a konkretnie tego, co dzieje się, gdy łączy się on ze swoim receptorem, białkiem znanym jako LDLR. Zazwyczaj, gdy LDL wiąże się z LDLR, rozpoczyna się proces usuwania LDL z krwi. Mutacje genetyczne mogą jednak uniemożliwić tę pracę, powodując gromadzenie się LDL we krwi i osadzanie się w tętnicach w postaci płytki nazębnej, co może prowadzić do miażdżycy, będącej prekursorem chorób serca.
W nowym badaniu naukowcom udało się wykorzystać najnowocześniejszą technologię, aby uzyskać wgląd w to, co dzieje się na krytycznym etapie tego procesu i spojrzeć na LDL w nowym świetle.
„LDL jest ogromny i ma różną wielkość, co czyni go bardzo złożonym” – wyjaśnił dr Joseph Marcotrigiano, kierownik Sekcji Wirusologii Strukturalnej w Laboratorium Chorób Zakaźnych w Narodowym Instytucie Alergii i Chorób Zakaźnych NIH oraz współautor na badaniu. „Nikt nigdy nie osiągnął takiego rozwiązania, jakie my mamy. Mogliśmy zobaczyć tak wiele szczegółów i zacząć rozgryzać, jak to działa w organizmie.
Zaawansowane techniki odkrywają nowe spostrzeżenia
Korzystając z zaawansowanej techniki obrazowania zwanej mikroskopią krioelektronową, badaczom udało się zobaczyć całe białko strukturalne LDL, gdy jest ono związane z LDLR. Następnie, korzystając z oprogramowania do przewidywania białek opartego na sztucznej inteligencji, udało im się modelować strukturę i zlokalizować znane mutacje genetyczne, które powodują zwiększenie poziomu LDL. Twórcy oprogramowania, którzy nie brali udziału w badaniu, otrzymali niedawno Nagrodę Nobla w dziedzinie chemii za rok 2024.
Naukowcy odkryli, że wiele mutacji przypisanych do miejsca połączenia LDL i LDLR było powiązanych z chorobą dziedziczną zwaną hipercholesterolemią rodzinną (FH). FH charakteryzuje się zaburzeniami wchłaniania LDL przez organizm do komórek, a osoby z nią mają niezwykle wysoki poziom LDL i mogą mieć zawał serca w bardzo młodym wieku. Odkryli, że warianty związane z FH mają tendencję do skupiania się w określonych regionach LDL.
Wyniki badania mogą otworzyć nowe możliwości opracowania terapii celowanych mających na celu korygowanie tego rodzaju dysfunkcyjnych interakcji spowodowanych mutacjami. Co jednak ważne, jak stwierdzili naukowcy, mogą one również pomóc osobom, które nie mają mutacji genetycznych, ale mają wysoki poziom cholesterolu i przyjmują statyny, które obniżają poziom LDL poprzez zwiększenie poziomu LDLR w komórkach. Wiedząc dokładnie, gdzie i jak LDLR wiąże się z LDL, naukowcy twierdzą, że mogą teraz być w stanie namierzyć te punkty połączenia, aby zaprojektować nowe leki obniżające poziom LDL we krwi.
Odniesienie: „Struktura apolipoproteiny B100 związanej z receptorem lipoprotein o niskiej gęstości” autorstwa: Mart Reimund, Altaira D. Dearborn, Giorgio Graziano, Haotian Lei, Anthony M. Ciancone, Ashish Kumar, Ronald Holewinski, Edward B. Neufeld, Francis J. O’Reilly, Alan T. Remaley i Joseph Marcotrigiano, 11 grudnia 2024 r., Natura.
DOI: 10.1038/s41586-024-08223-0
Prace te były wspierane przez programy badań stacjonarnych Narodowego Instytutu Serca, Płuc i Krwi, Narodowego Instytutu Alergii i Chorób Zakaźnych, Narodowego Instytutu Raka oraz program High-Value Datasets prowadzony przez Biuro ds. Strategii Nauki o Danych NIH.