Naukowcy odkryli, że psilocybina, aktywny związek grzybów magicznych, zakłóca sieci introspektywne mózgu, w szczególności desynchronizując sieć trybu domyślnego. Zmiana ta powoduje głębokie skutki psychologiczne i może mieć trwały wpływ na elastyczność mózgu i zdrowie psychiczne. Ich odkrycia sugerują potencjalne zastosowania terapeutyczne psilocybiny w leczeniu schorzeń takich jak depresja i zespół stresu pourazowego (PTSD). Źródło: SciTechDaily.com
Nowe badania przyspieszają wysiłki mające na celu wykorzystanie zmieniającej umysł mocy leku w leczeniu chorób psychicznych.
Nowe badanie to pokazuje psilocybina, aktywny związek magicznych grzybów, wpływa na mózg, tymczasowo zmieniając krytyczne sieci introspektywne, co może prowadzić do głębokich przemian psychologicznych. Odkrycia te wskazują na potencjalne zastosowania psilocybiny w opracowywaniu metod leczenia zaburzeń zdrowia psychicznego, takich jak depresja.
Osoby spożywające grzyby zawierające psilocybinę – inaczej zwane grzybami magicznymi – zazwyczaj przechodzą surrealistyczne doświadczenie, podczas którego ich poczucie przestrzeni, czasu i siebie zostaje zniekształcone. Zwolennicy od dawna argumentują, że w odpowiednich warunkach doznania psychedeliczne mogą złagodzić cierpienie psychiczne, a garść badań naukowych sugeruje, że mogą mieć rację. Dokładne zrozumienie wpływu leku na mózg pomoże naukowcom i lekarzom wykorzystać jego potencjał terapeutyczny.
W nowym badaniu naukowcy z Washington University School of Medicine w St. Louis donoszą, że psilocybina, substancja czynna zawarta w magicznych grzybach, tymczasowo zakłóca krytyczną sieć obszarów mózgu zaangażowanych w myślenie introspektywne, takie jak śnienie na jawie i zapamiętywanie. Odkrycia dostarczają neurobiologicznego wyjaśnienia oszałamiającego działania leku i kładą podwaliny pod opracowanie opartych na psilocybinie terapii chorób psychicznych, takich jak depresja i zespół stresu pourazowego.
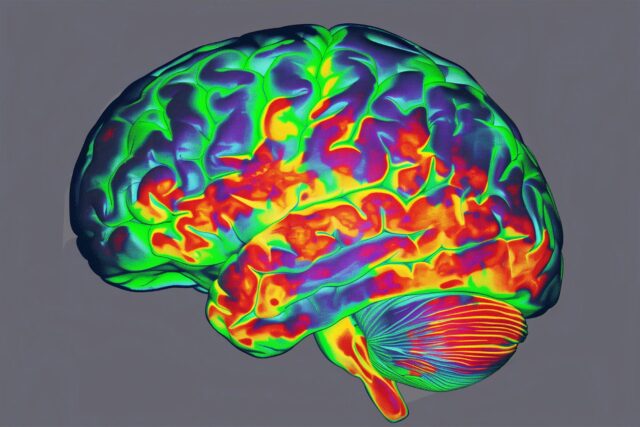
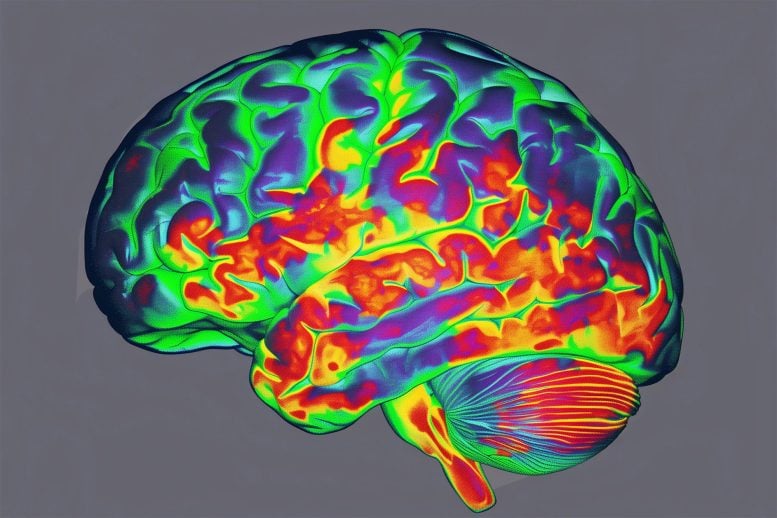
Ta mapa cieplna wzorców aktywności mózgu pokazuje głębokie zaburzenia podczas indywidualnych doświadczeń po zażyciu psilocybiny. Stosunkowo stabilne wzorce przed i po dawce (odcienie niebieski i zielony) są chwilowo zakłócane podczas „podróży” (odcienie czerwony, pomarańczowy i żółty). Naukowcy z Washington University School of Medicine w St. Louis donoszą, że psilocybina destabilizuje krytyczną sieć obszarów mózgu zaangażowanych w myślenie introspektywne. Odkrycia dostarczają neurobiologicznego wyjaśnienia oszałamiającego działania leku. Źródło: Sara Moser/Uniwersytet Waszyngtoński
„Początkowo efekt jest ogromny, a kiedy znika, pozostaje precyzyjny efekt” – powiedział współautor Nico UF Dosenbach, lekarz medycyny, profesor neurologii. „To jest dokładnie to, co chciałbyś zobaczyć w przypadku potencjalnego leku. Nie chciałbyś, aby sieci mózgowe ludzi zostały zniszczone na kilka dni, ale nie chciałbyś też, aby wszystko natychmiast wróciło do poprzedniego stanu. Chcesz efektu, który utrzyma się wystarczająco długo, aby coś zmienić.
Badanie, opublikowane 17 lipca w Naturatworzy plan działania, którym inni naukowcy mogą się kierować, aby ocenić wpływ leków psychoaktywnych na funkcjonowanie mózgu, potencjalnie przyspieszając prace nad opracowaniem leków na dowolną liczbę chorób psychicznych.
Kontekst historyczny i odnowione zainteresowanie
Psilocybina okazała się obiecująca w leczeniu depresji w latach pięćdziesiątych i sześćdziesiątych XX wieku, ale restrykcyjna federalna polityka narkotykowa w kolejnych dziesięcioleciach unieważniła prawie wszystkie dalsze badania. W ostatnich latach przepisy uległy jednak rozluźnieniu i zainteresowanie tą dziedziną ożyło.
„W dzisiejszych czasach dużo wiemy o skutkach psychologicznych i molekularnych/komórkowych psilocybiny” – powiedział pierwszy autor Joshua S. Siegel, lekarz medycyny, instruktor psychiatrii. „Ale niewiele wiemy o tym, co dzieje się na poziomie łączącym te dwa elementy – poziomie funkcjonalnych sieci mózgowych”.
Naukowcy z Washington University School of Medicine w St. Louis donoszą, że psilocybina destabilizuje krytyczną sieć obszarów mózgu zaangażowanych w myślenie introspektywne. Odkrycia dostarczają neurobiologicznego wyjaśnienia oszałamiającego działania leku. Źródło: Sara Moser/Uniwersytet Waszyngtoński
Metodologia i ustalenia
Aby wypełnić tę lukę, Siegel powołał zespół, w skład którego wchodził Dosenbach, ekspert w dziedzinie obrazowania mózgu, oraz współautorka Ginger E. Nicol, MD, profesor nadzwyczajny psychiatrii, który ma doświadczenie w prowadzeniu badań klinicznych z substancjami kontrolowanymi. Wspólnie opracowali sposób wizualizacji wpływu psilocybiny na funkcjonalne sieci mózgowe poszczególnych uczestników – neuronowe ścieżki komunikacji łączące różne obszary mózgu – i korelowania zmian w tych sieciach z subiektywnymi doświadczeniami.
Zespół zrekrutował siedmiu zdrowych dorosłych, aby przyjęli w kontrolowanych warunkach dużą dawkę psilocybiny lub metylofenidatu, generycznej formy Ritalinu. Ponieważ podróże psychodeliczne niosą ze sobą ryzyko, że użytkownicy będą mieli negatywne lub przerażające doświadczenia, para przeszkolonych ekspertów towarzyszyła każdemu uczestnikowi przez cały czas trwania doświadczenia. Eksperci pomogli przygotować uczestników na to, czego prawdopodobnie doświadczyli, zapewnili wskazówki i wsparcie podczas każdego eksperymentu, a także pomogli ochotnikom przetrawić to, co wydarzyło się później. Każdy uczestnik przeszedł średnio 18 funkcjonalnych skanów mózgu MRI w dniach lub tygodniach przed, w trakcie i do trzech tygodni po doświadczeniach z psilocybiną. Czterech uczestników wróciło sześć miesięcy później, aby powtórzyć eksperyment.
Wpływ na funkcjonowanie mózgu i postrzeganie siebie
Psilocybina spowodowała głębokie i powszechne – choć nie trwałe – zmiany w sieciach funkcjonalnych mózgu. W szczególności zdesynchronizowało sieć trybu domyślnego, czyli połączony zestaw obszarów mózgu, które zwykle są jednocześnie aktywne, gdy mózg nie pracuje nad niczym szczególnym. Po utracie synchronizacji sieć odbudowała się, gdy ustały ostre skutki narkotyku, ale niewielkie różnice w porównaniu ze skanami przed psilocybiną utrzymywały się przez tygodnie. Sieć trybu domyślnego pozostała stabilna u osób, które otrzymały metylofenidat.
„Chodzi o to, że bierzesz pod uwagę system, który ma fundamentalne znaczenie dla zdolności mózgu do myślenia o sobie w odniesieniu do świata, i tymczasowo całkowicie go desynchronizujesz” – powiedział Siegel. „Na krótką metę tworzy to psychodeliczne doświadczenie. Długoterminową konsekwencją jest to, że mózg staje się bardziej elastyczny i potencjalnie ma większą zdolność do powrotu do zdrowszego stanu”.
Zwykle funkcjonalna sieć mózgowa każdego człowieka jest tak charakterystyczna jak odcisk palca. Psylocybina zniekształciła sieci mózgowe tak dokładnie, że nie można było już zidentyfikować poszczególnych osób, dopóki nie ustały ostre efekty.
„Mózgi ludzi na psilocybinie są bardziej podobne do siebie niż do swojej nieporuszonej jaźni” – stwierdził Dosenbach. „Ich indywidualność zostaje chwilowo zatarta. To weryfikuje, na poziomie neuronaukowym, co ludzie mówią o utracie poczucia siebie podczas podróży”.
Implikacje dla psychiatrii
Podczas doświadczenia uczestnicy zostali poproszeni o ocenę swoich uczuć transcendencji, połączenia i podziwu, korzystając z zatwierdzonego Kwestionariusza Doznania Mistycznego. Wielkość zmian w sieciach funkcjonalnych śledzona za pomocą intensywności subiektywnego doświadczenia każdego uczestnika.
„Udało nam się uzyskać bardzo dokładne dane na temat wpływu leku na każdą osobę” – powiedziała Nicol. „To krok w kierunku precyzyjnych badań klinicznych. W psychiatrii często nie wiemy, kto powinien otrzymać dany lek, w jakiej ilości i jak często. W rezultacie przepisujemy jeden lek za drugim, majstrując przy dawkowaniu, aż znajdziemy coś, co działa. Stosując to podejście w badaniach klinicznych, możemy zidentyfikować czynniki decydujące o tym, kto odniesie korzyść, a kto nie, i lepiej wykorzystać dostępne leki”.
Nicol, Siegel i Dosenbach podkreślają, że ludzie nie powinni interpretować swoich badań jako powodu do samoleczenia psilocybiną. Lek nie został zatwierdzony przez Agencję ds. Żywności i Leków (FDA) do leczenia depresji lub innych schorzeń, a jego przyjmowanie bez nadzoru przeszkolonych ekspertów w dziedzinie zdrowia psychicznego wiąże się z ryzykiem.
Odniesienie: „Psilocybina desynchronizuje ludzki mózg” Joshua S. Siegel, Subha Subramanian, Demetrius Perry, Benjamin P. Kay, Evan M. Gordon, Timothy O. Laumann, T. Rick Reneau, Nicholas V. Metcalf, Ravi V. Chacko , Caterina Gratton, Christine Horan, Samuel R. Krimmel, Joshua S. Shimony, Julie A. Schweiger, Dean F. Wong, David A. Bender, Kristen M. Scheidter, Forrest I. Whiting, Jonah A. Padawer-Curry, Russell T. Shinohara, Yong Chen, Julia Moser, Essa Yacoub, Steven M. Nelson, Luca Vizioli, Damien A. Fair, Eric J. Lenze, Robin Carhart-Harris, Charles L. Raison, Marcus E. Raichle, Abraham Z. Snyder , Ginger E. Nicol i Nico UF Dosenbach, 17 lipca 2024 r., Natura.
DOI: 10.1038/s41586-024-07624-5